



Unsere Peptidbibliothek

Peptide sind kurze Ketten von Aminosäuren, die durch Peptidbindungen verbunden sind und typischerweise aus 2 bis 50 Aminosäuren bestehen. Sie sind strukturell kleiner als Proteine und werden oft als kleine oder Miniproteine bezeichnet. Peptide spielen vielfältige und wesentliche Rollen in biologischen Systemen und fungieren als Hormone, Neurotransmitter, antimikrobielle Wirkstoffe, Signalmoleküle und Enzymregulatoren usw. Ihre Fähigkeit, gezielt mit biologischen Zielen zu interagieren, macht sie in der Medizin, Biotechnologie und industriellen Anwendungen von unschätzbarem Wert. Daher werden Peptide häufig als Therapeutika, Kosmetika und Forschungsinstrumente eingesetzt.
Die Entdeckung und Entwicklung neuartiger Peptide für diese Anwendungen erfordert effiziente Screening-Methoden. Eine der wirkungsvollsten Strategien ist die Verwendung von Peptidbibliotheken. Eine Peptidbibliothek ist eine Sammlung verschiedener Peptide, die für das Hochdurchsatz-Screening in der biochemischen und pharmazeutischen Forschung konzipiert sind. Diese Bibliotheken sind maßgeblich an der Untersuchung von Protein-Protein-Wechselwirkungen, der Enzym-Substrat-Spezifität, der Arzneimittelentwicklung und der Epitopkartierung beteiligt. Durch systematische Variation von Peptidsequenzen und -strukturen können Forscher bioaktive Peptide mit wünschenswerten Eigenschaften für therapeutische und industrielle Anwendungen identifizieren.
Peptidbibliotheken können grob in zwei Typen eingeteilt werden:
Synthetische Peptidbibliotheken
Diese Bibliotheken werden mithilfe der Festphasen-Peptidsynthese (SPPS) erstellt und ermöglichen eine präzise Kontrolle der Peptidsequenzen. Sie können nach dem Zufallsprinzip oder auf der Grundlage spezifischer interessierender Strukturen entworfen werden, was sie zu einem vielseitigen Werkzeug für Screening und Optimierung macht.
Biologische Peptidbibliotheken
Diese Bibliotheken werden mithilfe von Techniken wie Phagen-Display oder Ribosomen-Display generiert, bei denen Peptide entweder auf der Oberfläche von Bakteriophagen exprimiert oder mit ihrer kodierenden mRNA verknüpft werden. Diese Bibliotheken enthalten oft Milliarden bis Billionen von Peptidvarianten und bilden „Supermischungen“, die die Chancen zur Identifizierung wirksamer bioaktiver Peptide erheblich erhöhen.
Aktuelle globale Peptidbibliotheken stehen vor mehreren kritischen Herausforderungen, darunter:
Begrenzte strukturelle Vielfalt
Die meisten Bibliotheken bestehen nur aus einer einzigen Art von Peptidstruktur, was den Umfang potenzieller Entdeckungen verringert.
Low-Sequenz-Diversität
Ein begrenzter Bereich an Sequenzen schränkt die Fähigkeit ein, neue bioaktive Peptide zu identifizieren.
Komplexe mischungsbasierte Bibliotheken
Auf Supermischungen basierende Bibliotheken enthalten Hunderte Millionen Peptide in hochkomplexen Pools, was die effiziente Erfassung hochwertiger aktiver Peptide erschwert.
PeptiOrigins innovative 3D-strukturierte Peptidbibliothek bietet beispiellose Funktionen und ist darauf ausgelegt, diese Herausforderungen zu bewältigen, darunter:
Peptidsequenzvielfalt auf Billionenebene ermöglicht umfassende Erforschung bioaktiver Kandidaten.
Die Einbeziehung aller fünf Hauptpeptidstrukturen erweitert die strukturelle Vielfalt erheblich.
Ein Nicht-Super-Mischungs-Design, das hohe Screening-Erfolgsraten und eine schnellere Entdeckung aktiver Peptide gewährleistet.
Vielseitigkeit für alle Ziele und Screening-Modelle, wodurch es für verschiedene Forschungs- und Therapieanwendungen geeignet ist.
Durch die Nutzung der Peptidbibliothek von PeptiOrigin können Forscher die Entwicklung innovativer peptidbasierter Therapeutika und Biomoleküle beschleunigen und so den Fortschritt in der Arzneimittelforschung vorantreiben.
Sequenzvielfalt
Prinzipien unseres Big-Data-gesteuerten Peptidsequenzdesigns

Enthält nicht-natürliche Aminosäuren für überlegene Peptideigenschaften.
Unsere Peptidbibliothek verfügt über eine beispiellose Sequenzvielfalt und ermöglicht die Entdeckung hochaffiner, funktionsoptimierter Peptidkandidaten für die Arzneimittelentwicklung, die Entdeckung von Biomarkern und gezielte Therapien.
Strukturvielfalt
Bioaktive Peptide weisen sowohl Sequenz- als auch Strukturvielfalt auf, was bedeutet, dass ihre Aminosäurezusammensetzung und dreidimensionale Konformation gemeinsam ihre biologischen Aktivitäten beeinflussen. Beispiele hierfür sind lineare Peptide wie Glutathion und Aspartam, zyklische Peptide wie Octreotid und komplexere Strukturen wie Vancomycin und Ziconotid mit drei Ringen. Diese strukturellen Variationen sind der Schlüssel zu ihrer Bioaktivität.
Strukturelle Unterschiede in Peptiden wirken sich erheblich auf ihre physikalisch-chemischen Eigenschaften aus, wie z. B. Löslichkeit, Permeabilität, Lipophilie und gesamte polare Oberfläche. Darüber hinaus haben diese Variationen großen Einfluss auf die Bindungskapazität, funktionelle Aktivität oder Selektivität von Peptiden gegenüber ihren Zielen.
Derzeit weisen die meisten Peptidbibliotheken auf dem Markt nur einen Strukturtyp auf – entweder linear, zyklisch oder bizyklisch. Während diese Bibliotheken die Entdeckung einiger bioaktiver Peptide erleichtert haben, schränkt ihre begrenzte strukturelle Vielfalt die Möglichkeiten zur Entdeckung neuer bioaktiver Moleküle erheblich ein.
Unsere Bibliothek umfasst Peptide mit verschiedenen 3D-Strukturen: lineare, zyklische, bizyklische, trizyklische und tetrazyklische Strukturen sowie über 10 neuartige Strukturen, die in der Natur nicht vorkommen. Diese Innovationen verbessern die Bindungsaffinität, Spezifität, Stabilität und sogar die orale Verfügbarkeit und machen die Bibliothek ideal für die Arzneimittelforschung.
Linear
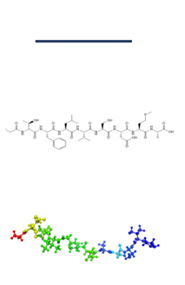
Leuprolid
Teriparatid
Semaglutid
Zyklisch
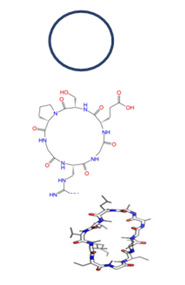
Octreotid
Oxytocin
Gemischt
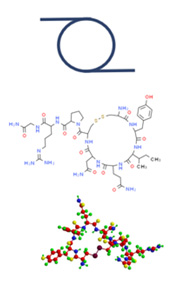
Vasopressin
Daptomycin
Insulin
Bizyklisch
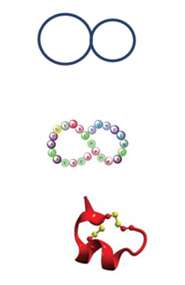
Endothelin
Vancomycin
Trizyklisch
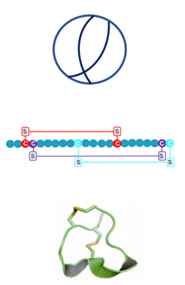
Ziconotid
μ-Conotoxin
Peptide, insbesondere natürliche, bilden einzigartige 3D-Strukturen, die für ihre Bioaktivitäten von entscheidender Bedeutung sind.
Größenvielfalt
Die Größenvielfalt in einer Peptidbibliothek ist aus mehreren Gründen von entscheidender Bedeutung:
Verbesserte Abdeckung potenzieller Ziele:
Unterschiedliche Peptidgrößen interagieren auf einzigartige Weise mit biologischen Zielen. Kürzere Peptide können auf flache Bindungstaschen zugreifen, während längere Peptide mit größeren oder komplexeren Oberflächen interagieren können. Durch die Größenvielfalt wird sichergestellt, dass ein breiteres Spektrum potenzieller Ziele angesprochen wird.
Maximierte funktionale Vielfalt:
Die Peptidgröße beeinflusst die strukturelle und funktionelle Vielfalt. Kürzere Peptide sind einfacher und können kleine molekulare Motive nachahmen, während längere Peptide komplexe Sekundär- und Tertiärstrukturen annehmen können, die vielfältige biologische Aktivitäten bieten.
Minimierte Entwicklungsrisiken:
Durch die Größenvielfalt können Forscher Kandidaten mit dem besten Gleichgewicht zwischen Wirksamkeit, Stabilität und Herstellbarkeit identifizieren und so das Risiko eines Scheiterns während der Entwicklung verringern.
Minimierte Immunogenität:
Die Peptidgröße spielt eine entscheidende Rolle bei der Immunogenität und sollte für die Arzneimittelentwicklung minimiert werden. Größere Peptide, insbesondere solche mit mehr als 12–15 Aminosäuren, lösen mit größerer Wahrscheinlichkeit eine Immunantwort aus. Daher ist die Kontrolle der Peptidgröße für die Reduzierung des Immunogenitätsrisikos von entscheidender Bedeutung.
Verbesserte Screening-Effizienz:
Die Einbeziehung von Peptiden unterschiedlicher Länge erhöht die Wahrscheinlichkeit, Peptide mit optimalen Eigenschaften für ein bestimmtes Ziel zu entdecken, wie z. B. Bindungsaffinität, Spezifität oder Stabilität.
Kurze Peptide bieten den Vorteil niedriger Herstellungskosten und minimaler bis keiner Immunogenität, was sie ideal für den langfristigen Einsatz als neue Medikamente macht. Unsere Bibliothek umfasst Peptide mit 2 bis 20 Aminosäuren und bietet so eine vielfältige Auswahl.
2 aa: 202 = 400
3 aa: 203 = 8.000
4 aa: 204 = 160.000
5 aa: 205 = 3.200.000
6 aa: 206 = 64.000.000
Unsere Bibliothek enthält:
Alle Dipeptide
Alle Tripeptide
Alle Tetrapeptide
Alle Pentapeptide
Alle Hexapeptide
Peptide mit einer Länge von 7 bis 20 Aminosäuren, die durch die Anwendung mathematischer Prinzipien zur Maximierung der Sequenzvielfalt entwickelt wurden.
Nicht-Super-Mischungsbibliothek
Bestehende kombinatorische Chemie- und Phagen-Display-Bibliotheken sind für ihre große Kapazität (Billionen) und hohe Screening-Effizienz bekannt, die das Screening von Billionen von Peptiden in einer einzigen Runde ermöglicht. Allerdings weisen diese Bibliotheken trotz ihrer weiten Verbreitung erhebliche Einschränkungen auf.
Supermischung aus Milliarden oder Billionen Peptiden


Nachteile:
Eine extrem niedrige Peptidkonzentration verringert die Wahrscheinlichkeit, optimale Kandidaten zu identifizieren.
Signifikante und unvermeidbare Peptidinteraktionen können zu falsch positiven und falsch negativen Ergebnissen führen.
Eine begrenzte Strukturvielfalt in Bibliotheken schränkt die Entdeckung neuer bioaktiver Peptide ein.
Komplexe Peptidmischungen in Bibliotheken können ein effizientes und genaues Screening behindern und sie für bestimmte Methoden wie Phänotyp- oder zellbasiertes Screening ungeeignet machen.
Unsere Nicht-Supermischungsbibliothek enthält 200.000 kleine Peptidbibliotheken, von denen jede 1 bis Tausende verschiedene Peptide enthält, was die Falsch-Positiv-Raten und Falsch-Negativ-Raten deutlich reduziert, was zu einem höheren Screening-Erfolg und einer schnelleren Entdeckung aktiver Peptide führt. Die Bibliothek eignet sich auch für beliebige Screening-Modelle oder -Methoden wie Phänotyp-Screening oder zellbasierte Assays.
Fluorescein-markierte Peptide
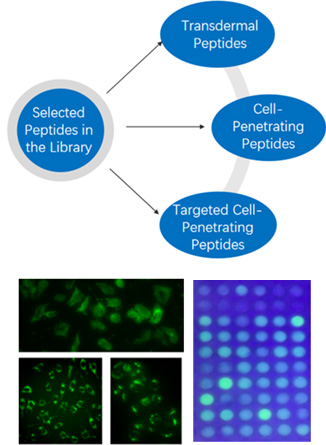
Peptide wie zellpenetrierende Peptide, zielgerichtete zellpenetrierende Peptide und transdermale Peptide enthalten häufig einen höheren Anteil an basischen Aminosäuren wie Arginin und Lysin. Diese Peptide tragen im menschlichen Körper eine positive Ladung und können sich so an negativ geladene Phosphatgruppen auf Zellmembranen binden – eine Schlüsselvoraussetzung für das Durchdringen der Membran.
Darüber hinaus tragen Aminosäuren wie Tyrosin, Tryptophan und Phenylalanin erheblich zur Membranpenetration bei, gefolgt von hydrophoben Aminosäuren wie Leucin und Isoleucin. Umgekehrt stoßen saure Aminosäuren aufgrund ihrer negativen Ladung die Phosphatgruppen auf der Membran ab, wodurch sie für die Transmembranaktivität ungünstiger werden.
Basierend auf diesen Prinzipien und der Expertise des Unternehmens im Design von Peptidbibliotheken werden ausgewählte Peptide in der Bibliothek fluoreszierend markiert, um ein effizientes Screening von zellpenetrierenden Peptiden, zielgerichteten zellpenetrierenden Peptiden und transdermalen Peptiden zu ermöglichen.
Wir nutzen unsere proprietäre, umfangreiche Peptidbibliothek, um umfassende CRO-Dienste für die Entdeckung von Peptidwirkstoffen bereitzustellen.
Kontakt
Wir freuen uns über Ihre Anfragen und Ihr Feedback! Egal, ob Sie weitere Informationen zu unserer Peptidbibliothek, unseren Dienstleistungen oder Möglichkeiten zur Zusammenarbeit suchen, unser Team steht Ihnen gerne zur Seite.
Hauptmerkmale unserer Peptidbibliothek-Plattform

Cookies
We use cookies to ensure that we give you the best experience on and off our website. please review our privacy policy

